

本制品是一种通过化学发光法测定细胞内ATP含量从而用于超高灵敏度、超宽线性范围定量检测活细胞数目的试剂盒。
本制品是CellTic-Lumi(简称CTL)的不同包装版本,两者的检测效果完全一致。CTL为即用型液体,优点是无需配制即可以直接使用,缺点是长期保存需要置于-80℃,如果在-20℃保存时间较长后检测效果会逐渐下降;本制品(简称CTL II)为CTL的冻干粉版本,使用前需要使用提供的缓冲液充分溶解底物冻干粉后才能使用,优点是在-20℃保存特别稳定。
本试剂盒的性能基本达到甚至在有些方面优于国外同类产品。本制品的用途与CTL Plus及Promega公司的CellTiter-Glo基本相同,检测灵敏度和发光检测数据略优于CTL Plus,显著优于CellTiter-Glo,线性范围和CTL Plus和CellTiter-Glo相近,但检测上限和发光检测数据随时间的稳定性稍稍低于CTL Plus和CellTiter-Glo。

本试剂盒通过ATP检测细胞活力的原理图。借助ATP依赖的萤光素酶催化的萤光素发光反应,ATP可以通过测定化学发光来进行定量。由于ATP含量能很好地反映活细胞的数目,而ATP含量和发光强度成正比,这样就可以简单地通过化学发光强度来计算出细胞活力或细胞数目。


ATP作为最重要的能量分子,在细胞的各种生理、病理过程中起着重要作用。ATP是细胞新陈代谢的一个重要指标,也是具有代谢活性细胞的重要标志性分子,并和活细胞数目成良好的线性关系。因此,ATP含量能很好地反应活细胞的数目,即本试剂盒可以通过测定ATP含量来进行细胞计数或检测细胞活力。

- 线性范围宽:96孔板中,在12个至3万个细胞范围内有良好的线性关系。不同细胞的检测数量上限会有显著不同,对于一些ATP含量特别高的细胞,在细胞数量达到3万个后可能会不呈现线性关系,但化学发光读数还是会继续升高的。如果检测的细胞数量超过3万,推荐使用检测上限更高的CellTic-Lumi Plus II发光法细胞活力检测试剂盒或CellTic-Lumi Plus化学发光法细胞活力检测试剂盒。
- 发光强度高:对于相同的细胞样品,通常在3万个细胞数量范围内,本制品的发光效果比CTL Plus强约20~100%,比国外同类产品强1~3倍,实测效果会因细胞种类的不同而有所不同。例如,对于NIH3T3和HeLa细胞的检测,CTL的发光强度比CTL Plus高约40~100%,比国外同类产品强约2~3倍;而对于Jurkat细胞的检测,CTL的发光强度则比CTL Plus强约20~70%,比国外同类产品强约1.5~3倍)。
- 检测灵敏度高:使用本制品检测细胞数量仅为12个/孔时,发光强度可达空白孔的2倍左右。
- 检测速度快:操作简单,读数稳定,完成检测仅需约10分钟。本制品比常见的MTT、alamarBlue、Calcein-AM、WST-1、CCK-8等其它细胞活力测定方法更加简单快捷。只需用试剂盒提供的检测缓冲液把检测底物(冻干粉)充分溶解后配制成CellTic-Lumi II发光法检测试剂后,与培养细胞等体积混合,反应10分钟后即可进行化学发光检测。无需洗涤细胞,也无需更换或去除培养液。并且化学发光比较稳定,在反应开始后的10分钟内下降不超过10%,30分钟内的下降不超过30%。
- 稳定性好:本制品在-20℃可以长期保存,配制成CellTic-Lumi II发光法检测试剂后的稳定性也非常好,反复冻融5次对检测效果基本无影响,反复冻融10次检测效果下降不超过10%。CellTic-Lumi II发光法检测试剂在4℃保存3天对检测效果无显著影响,保存7天检测效果下降不超过10%。在室温保存1天仍可保留80%以上的检测效果。在37℃保存1天可保持60%以上的检测效果。
- 使用灵活便捷:本制品不仅适合少量样品检测,也非常适合大量样品的高通量筛选检测。

| 组分 | 100T | 500T | 2500T | 10000T |
| CellTic-Lumi II发光法检测缓冲液 | 10mL | 50mL | 50mL×5 | 100mL×10 |
| CellTic-Lumi II发光法检测底物 | 1瓶 | 1瓶 | 5瓶 | 10瓶 |
保存:-20℃,避光,有效期2年。

检测缓冲液和检测底物混合后配制成的CellTic-Lumi II发光法检测试剂,-20℃避光保存,至少一年有效;-80℃避光保存,至少两年有效。

对于96孔板,推荐使用100μL细胞培养液和100μL的检测试剂,总体积为200μL,此时本试剂盒每10mL可以进行100次检测。对于384孔板,推荐使用25μL细胞培养液和25μL的检测试剂,总体积为50μL,此时本试剂盒每10mL可以进行400次检测。也可以用其它体积的试剂进行检测,但细胞培养液和检测试剂体积的比例须为1:1。

- 对于订购后可能放置较长时间后再使用的,或者对于检测结果的精度要求特别高的,推荐订购本制品,即CellTic-Lumi II;对于订购后短期内使用完毕的,推荐订购使用更加便捷的CellTic-Lumi化学发光法细胞活力检测试剂盒。
- 由于萤光素酶的活性对温度比较敏感,所以反应前细胞和检测试剂均需达到室温后再进行测定。可将检测缓冲液在不超过25℃的室温或20~25℃的水浴中融解并混匀后再与检测底物混合成检测试剂使用。
- 本试剂盒的检测缓冲液和检测底物混合后配制成的CellTic-Lumi II发光法检测试剂中含有萤光素酶,反复冻融会导致其逐渐失活。尽管经测试CellTic-Lumi II发光法检测试剂反复冻融5次对于其检测效果无显著影响,为保证检测试剂的稳定性、取得良好的使用效果,建议现用现配。没有用完的检测试剂可适当分装保存,但需注意分装的容器不能有ATP污染。反复冻融过程中,可能会导致检测试剂中出现少量沉淀,此时宜平衡至室温,并尽量溶解。如仍有残留的不溶物,可以离心去除后使用,经测试不会影响后续的检测效果。
- 待测药物的溶剂含量较高时可能会干扰萤光素酶反应,从而影响化学发光信号。可以通过设置含有溶剂的细胞培养液对照孔排除溶剂的干扰。经测试,最终反应体系中DMSO含量在2%以内不会对反应产生影响。
- 检测时需使用白色或黑色的96孔板或384孔板。如果使用普通透明的96孔板或384孔板,相邻孔之间会产生相互干扰。
- 使用说明中提供了检测ATP标准品的方法,实际检测细胞活力时通常并不需要检测ATP标准品。

- 细胞的准备:
使用适合进行化学发光检测的96孔板,每孔接种100μL细胞(如使用384孔板,每孔接种25μL细胞,具体用量视不同类型的384孔板而定),并确保检测时每孔的细胞数量在3万个以内(如使用384孔板宜控制在6千个以内),同时设置不含细胞的培养液孔作为阴性对照,按照细胞培养的常规方法培养细胞。如有需要,可加入药物处理细胞。此外,如有必要,也可以设置细胞的浓度梯度,以便后续确定试剂盒的使用效果。 - ATP标准曲线的设置(选做):
把自备的ATP标准溶液用PBS或细胞培养液稀释成适当的浓度梯度。初次检测可以设置0、1、3、10、30、100、300、1000、3000nM这几个浓度,96孔板每孔加入100μL的标准品。如有必要,在后续的实验中可以根据细胞中的ATP含量对标准品的浓度范围进行适当调整。如果用细胞培养液来稀释ATP标准品,稀释后需立即进行后续的发光检测,否则培养液中的ATPase等可以消耗ATP的酶会导致ATP含量下降。 - 检测试剂的准备:
- 融解冻存的CellTic-Lumi II发光法检测缓冲液,将检测缓冲液全部转移至检测底物瓶中,旋紧瓶盖后适当颠倒混匀,当检测底物全部溶解并混匀后即为CellTic-Lumi II发光法检测试剂。如有必要可适当分装配制好的检测试剂。经测试反复冻融5次对其检测效果无显著影响。
- 冻干粉状的CellTiter-Lum II发光法检测底物可能会有少量粘附在瓶盖和瓶口,旋开瓶盖前可以拿起瓶子用瓶底轻轻敲击桌面,使粉末尽量掉落至瓶底,然后再轻轻旋开瓶盖,并注意不要损失冻干粉。
- 按照96孔板每孔100μL (384孔板每孔25μL)的量,取适量CellTic-Lumi II发光法检测试剂,平衡至室温。
- 融解冻存的CellTic-Lumi II发光法检测缓冲液,将检测缓冲液全部转移至检测底物瓶中,旋紧瓶盖后适当颠倒混匀,当检测底物全部溶解并混匀后即为CellTic-Lumi II发光法检测试剂。如有必要可适当分装配制好的检测试剂。经测试反复冻融5次对其检测效果无显著影响。
- 细胞活力检测:
- 取出细胞培养板在室温平衡10分钟(通常不宜超过30分钟)。
- 96孔板每孔加入100μL CellTic-Lumi II发光法检测试剂(384孔板每孔25μL)。
- 室温振荡2分钟,以促进细胞的裂解。
- 室温(约25℃)孵育10分钟,使发光信号趋于稳定。
- 使用具有检测化学发光功能的多功能酶标仪进行化学发光检测。请根据仪器要求设置相应的参数,每个孔的检测时间一般为0.25~1秒或更长时间,具体需根据仪器的检测灵敏度进行适当的调整。
- 根据化学发光读数直接计算细胞的相对活力,或根据ATP标准曲线计算出ATP的量从而计算出细胞的相对活力。对于培养细胞和ATP标准品的检测效果可以参考图2和图3,细胞在0-30,000个细胞/孔的细胞密度范围内有良好的线性关系,ATP标准品0-3,000nM浓度范围有良好的线性关系。
- 检测效果因细胞的种类不同而有所不同,对于一些ATP含量特别高的细胞,在细胞数量达到30,000个后可能会不呈现线性相关,但化学发光读数还是会继续升高的。
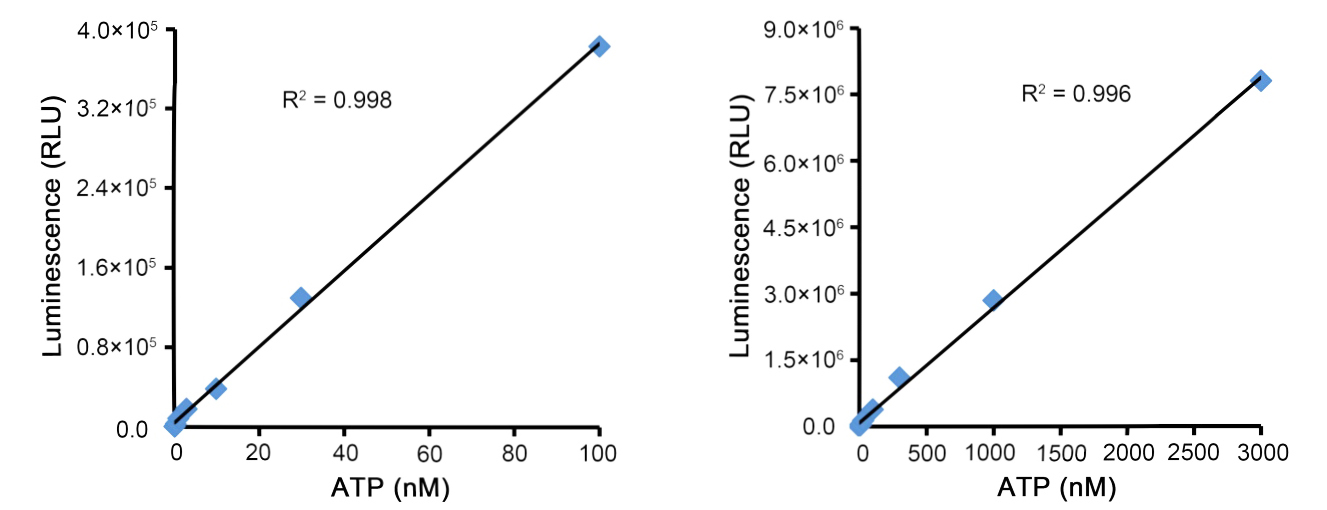
图2.CellTic-Lumi II发光法细胞活力检测试剂盒(CTL II)对ATP标准曲线的检测效果。实测数据会因检测仪器等的不同而存在差异,图中数据仅供参考。
- 取出细胞培养板在室温平衡10分钟(通常不宜超过30分钟)。

- Luminometer和荧光分光光度计有何不同?
荧光分光光度计检测的样品本身不能发光,样品需要由特定波长的激发光激发,然后才能产生荧光并被荧光分光光度计检测。Luminometer检测的样品本身可以发光,不需要激发光进行激发。也就是说luminometer是检测化学发光(萤光)的仪器。有些型号的荧光分光光度计也具有luminometer的功能,即也可以检测化学发光。您所使用的荧光分光光度计能否用于化学发光的测定请仔细阅读该仪器的说明书。 - 可以进行萤光素酶报告基因检测的仪器是否就可以用于本试剂盒的检测?
是。萤光素酶报告基因的检测原理和本试剂盒的原理相同,可以用相同的仪器测定。

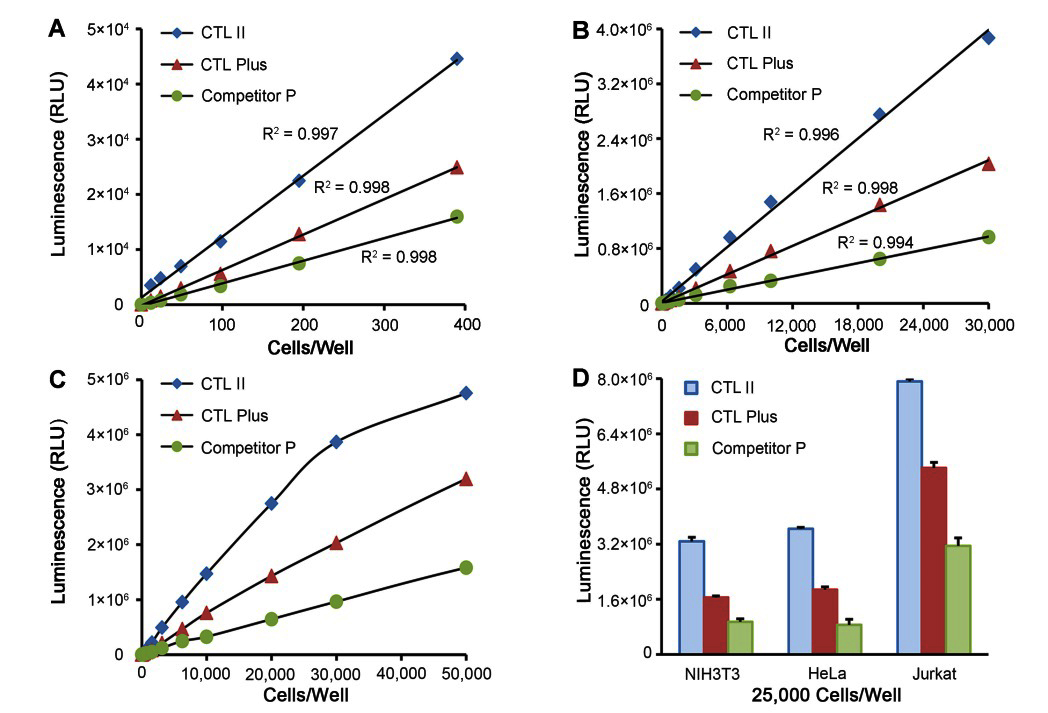
图3.CTL II和CTL Plus及国外同类产品Competitor P对不同细胞的检测效果。图A-C为CTL II、CTL Plus和Competitor P对不同数量HeLa细胞在白色96孔板中的检测效果,图D为CTL II、CTL Plus和Competitor P对2.5万个/孔NIH3T3、HeLa和Jurkat细胞在白色96孔板中的检测效果。实际读数会因细胞种类、检测仪器等的不同而存在差异,图中数据仅供参考。
相关搜索:CellTic-Lumi II细胞活力检测试剂盒(化学发光法),细胞内ATP含量检测,CTL II,活细胞数目定量检测,细胞活力检测



