

本制品是新一代的同源重组克隆试剂盒,精心优化的2×HiperClone Universal Enzyme Premix预混了重组酶和重组反应所需缓冲液,并添加了独特的重组增强因子,可显著提高重组克隆效率。
本试剂盒可以将PCR产物定向克隆至任何载体的任何位点,浓度可低至5ng/μL,一次可实现多至6个片段的顺序拼接克隆。将载体线性化,并在插入片段正、反向PCR引物5'端引入15~25bp的线性化载体末端同源序列,使得插入片段PCR产物5'和3'末端分别带有与线性化载体两末端对应的完全一致的序列。PCR产物和线性化载体在重组酶的作用下,仅需50℃,5~15min即可完成重组反应。克隆阳性率可达95%以上。

| 组分 | 20T | 50T |
| 2×HiperCloneUniversal Enzyme Premix | 200μL | 500μL |
| 500bp Control Insert (25ng/μL) | 5μL | 5μL |
| pUC19Control Vector,linearized (50ng/μL) | 5μL | 5μL |
保存:-20℃,有效期1年。

- 自备样品:自备好线性化载体和插入片段。
- 自备试剂(仅罗列部分):
- 超级感受态:转化效率>108cfu/μg。
- 高保真酶:高保真PCR Master Mix或其他等效产品。
- 菌落PCR mix:HiperPlus PCR Master Mix(含染料)或其他等效产品。
- 核酸染料:YoRed核酸染料(10000×)或其他等效产品。
- 超级感受态:转化效率>108cfu/μg。
- 自备仪器耗材(仅罗列部分):PCR仪,水平电泳槽,切胶仪,EP管等。

- 重组反应
- 线性化载体与插入片段使用量
HiperClone重组反应体系最适片段及载体插入总量为0.02~1pmol,1~3片段为0.02~0.5pmol,4~6片段为0.5-1pmol。最适载体与插入片段摩尔比为1:3。对应的DNA质量可由以下公式计算获得:线性化载体使用量ng=(线性化载体碱基对数×0.65×总pmol)/(1+3n)插入片段使用量ng=(插入片段碱基对数×0.65×总pmol×3)/(1+3n)其中n表示插入片段数目。- 当插入片段长度大于载体时,最适载体与插入片段使用量的计算方式应互换,即插入片段当做载体,载体当做插入片段进行计算。线性化载体及插入片段的使用量最低可达到5ng。线性化载体和插入片段扩增产物未纯化,直接使用时,使用总体积应不超过反应体系体积的1/5,如20μL体系不超过4μL。
- 重组反应体系(推荐冰上配制,各成分使用前需混匀)
成分 重组反应1~3片段 重组反应4~6片段 阴性对照 ddH2O 至20μL 至20μL 至20μL 2×HiperClone Universal Enzyme Premix 10μL 10μL 10μL 片段总量 0.02-0.5pmol 0.5-1pmol XμL - 重组反应条件
- 体系配制完成后,用移液器轻轻吸打混匀各组分,短暂离心将反应液收集至管底。
- 当插入1个片段并且DNA总量<300ng时,反应条件为50℃,5min;当插入片段数为2~6个时,建议反应条件为50℃,15~60min(反应时间随片段数增多而延长)。建议在PCR仪或金属浴等温控精确的仪器上进行反应。
- 反应产物可直接进行转化,也可储存于-20℃,待需要时解冻转化。
- 体系配制完成后,用移液器轻轻吸打混匀各组分,短暂离心将反应液收集至管底。
- 线性化载体与插入片段使用量
- 重组产物转化、涂板
- 在冰上解冻克隆感受态细胞。
- 取10μL冷却重组产物,加入到100μL感受态细胞中,轻弹管壁数下混匀,在冰上放置25min。
- 42℃热激50sec,冰浴孵育1~2min。
- 加入750μL SOC或LB培养基,37℃孵育2min充分复苏。37℃,200rpm,摇菌60min。
- 5000rpm离心3min,弃掉750μL上清。用剩余培养基将菌体重悬,用无菌涂布棒在含有正确抗性的平板上轻轻涂匀。
待菌液被吸收,将平板倒置,于37℃过夜培养。
- 在冰上解冻克隆感受态细胞。

- 单片段同源重组
一、实验流程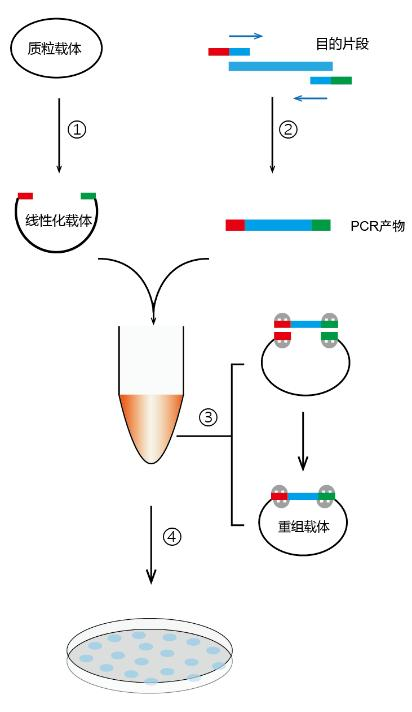
图1.HiperClone单片段同源重组实验流程图- 载体线性化:酶切或反向PCR制备线性化载体。
- 插入片段的制备:在目的片段正、反向引物的5'端引入15~25bp载体末端同源序列;PCR扩增目的片段,使得扩增产物5'和3'末端序列分别和线性化载体两末端序列完全一致。
- 重组反应:按比例混合线性化载体和插入片段,在重组酶催化作用下,50℃反应15min即可完成重组。
- 转化、涂板:将重组产物直接转化后涂平板。
二、制备线性化载体
选择合适的克隆位点,并对载体进行线性化。建议尽量选择无重复序列且GC含量均匀的区域进行克隆。载体克隆位点上下游25bp区域内GC含量均在40%~60%范围内最佳。线性化载体可通过限制性内切酶酶切或反向PCR扩增获得。- 酶切制备线性化载体
- 双酶切线性化:线性化完全,转化背景低。建议使用。
- 单酶切线性化:线性化程度较差。可适当延长酶切时间以降低转化背景。
- 不含插入片段的假阳性克隆可能是由未线性化环状载体转化而形成的。若这种假阳性克隆比例较高,建议重新制备线性化载体。
- 双酶切线性化:线性化完全,转化背景低。建议使用。
- 反向PCR扩增制备线性化载体
建议使用高保真聚合酶(如高保真PCR预混液)进行载体扩增,以减少扩增突变的引入。PCR扩增模板应尽量使用预线性化质粒,以防止残留环状质粒模板对克隆阳性率的影响。HiperClone重组反应体系兼容几乎所有酶切反应体系和常规PCR反应体系,当载体酶切产物或反向PCR扩增产物纯度较高时,可以无需纯化,直接进行重组反应。但纯度较低且有可能含有未线性化环状质粒时,建议使用高质量的试剂盒对线性化载体进行胶回收纯化,以提高产物纯度并去除一部分未线性化的环状载体,有利于提高重组效率。
三、PCR扩增制备插入片段- 设计扩增引物
HiperClone引物设计方式:通过在插入片段正、反向PCR引物的5'端引入15~25bp(不包括酶切位点)的线性化载体末端同源序列,使得插入片段PCR产物5'和3'末端分别带有与线性化载体两末端对应的完全一致的序列。
插入片段正向扩增引物设计方式:
5'—上游载体末端同源序列+酶切位点(可保留或删除)+基因特异性正向扩增引物序列—3'插入片段反向扩增引物设计方式:
3'—基因特异性反向扩增引物序列+酶切位点(可保留或删除)+下游载体末端同源序列—5'- 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 上游/下游载体末端同源序列为线性化载体最末端序列(用于同源重组),GC含量40%~60%为佳。
推荐使用无缝克隆引物设计软件,自动生成插入片段的扩增引物。若手动设计,可参照以下实例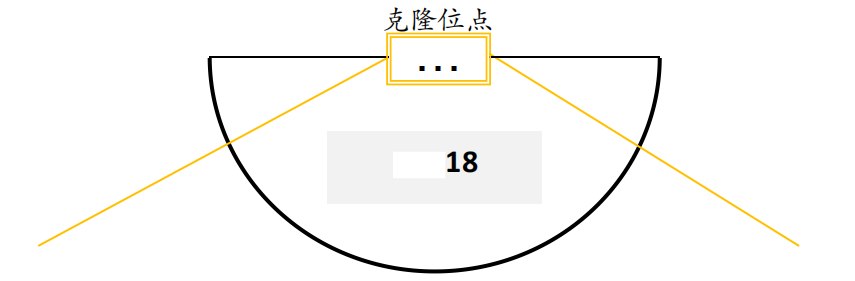
- 如载体选用双酶切线性化(Hind III + EcoR I):
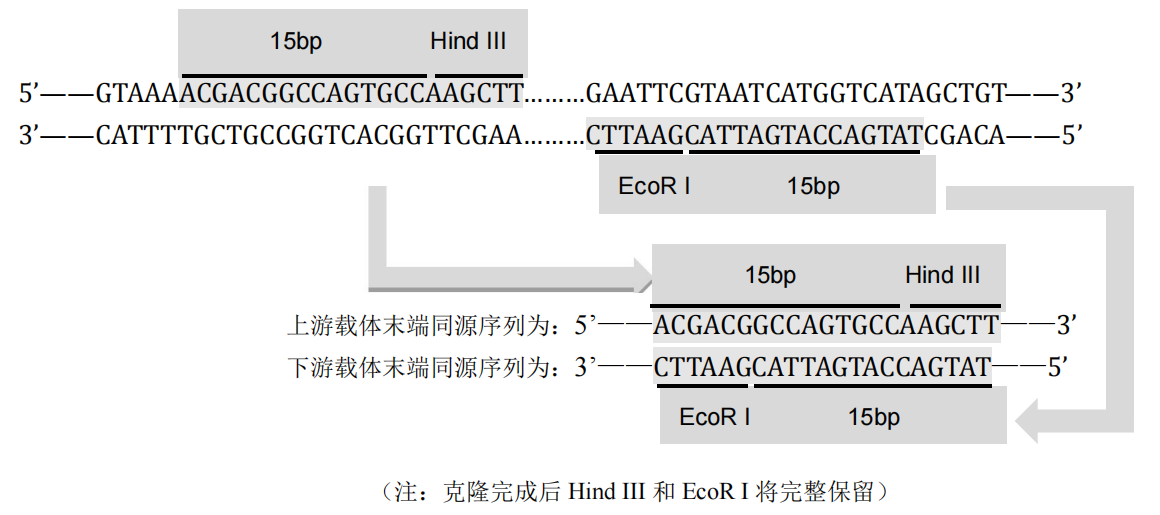
- 如载体选用单酶切线性化(BamH I):
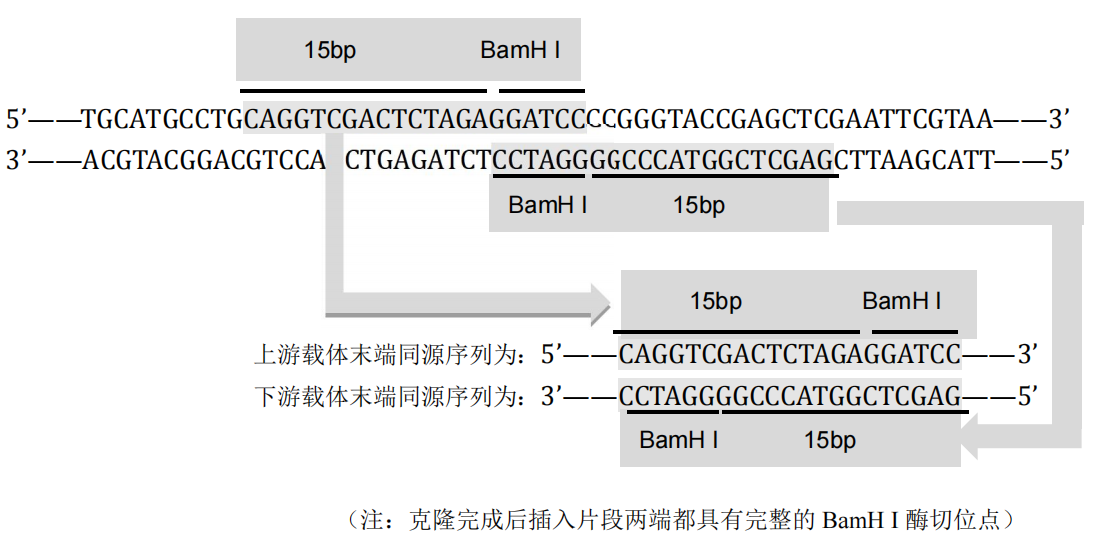
- 如载体选用反向PCR扩增制备:
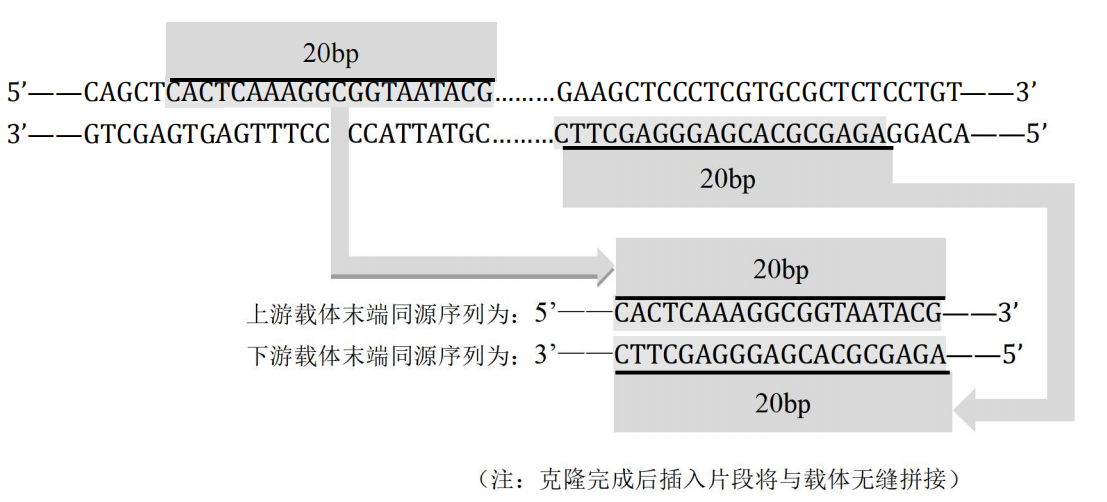
- 最终引物长度超过40bp,建议选用PAGE纯化方式进行引物合成。计算扩增引物退火温度时,只需计算基因特异性扩增序列的Tm值,载体末端同源序列不应参与计算,为了得到高效率克隆,建议Tm≥48℃。
- 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 插入片段PCR扩增
插入片段扩增可用任意PCR酶扩增,无需考虑产物末端有无A尾(重组过程中将被去除,在最终载体中不会出现)。但为了减少扩增突变的引入,建议使用高保真聚合酶进行扩增(如高保真PCR预混液)。
PCR扩增结束后,取少量产物进行琼脂糖凝胶电泳以检验扩增产量和特异性。HiperClone重组反应体系兼容常规PCR反应体系。因此,如果扩增模板不是与载体抗性相同的环状质粒,且PCR产物电泳条带单一,则扩增产物可以无需纯化,直接用于重组反应。但PCR扩增产物纯度较低时,建议使用高质量的试剂盒对PCR扩增产物进行胶回收纯化,以提高产物纯度,有利于提高重组效率。
- 载体线性化:酶切或反向PCR制备线性化载体。
- 多片段同源重组
一、实验流程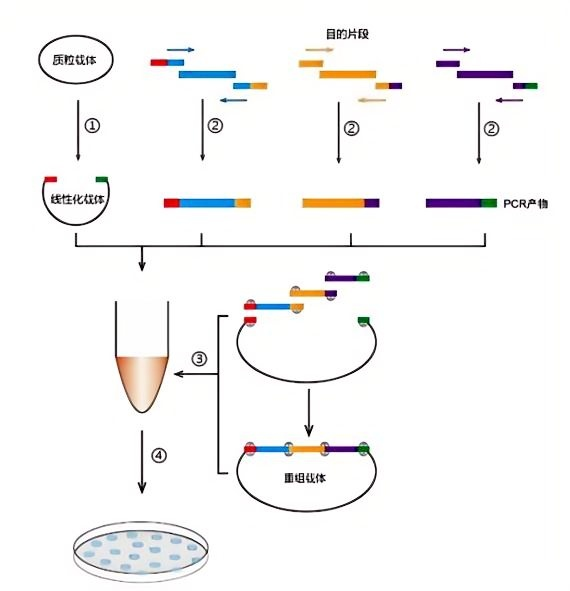
图3.HiperClone多片段同源重组实验流程图- 载体线性化:酶切或反向PCR制备线性化载体。
- 插入片段的制备:由PCR制备,所用扩增引物在设计时需在其5'端添加同源序列(图中以红色、黄色、紫色和绿色标记),使得扩增产物之间以及扩增产物与线性化载体之间各有一段同源序列。
- 重组反应:按比例混合线性化载体和插入片段,在重组酶催化作用下,50℃反应15min即可完成重组。
- 转化、涂板:将重组产物直接转化后涂平板。
- 载体线性化:酶切或反向PCR制备线性化载体。
二、制备线性化载体
选择合适的克隆位点,并对载体进行线性化。建议尽量选择无重复序列且GC含量均匀的区域进行克隆。载体克隆位点上下游25bp区域内GC含量均在40%~60%范围内最佳。线性化载体可通过限制性内切酶酶切或反向PCR扩增获得。
- 酶切制备线性化载体
- 双酶切线性化:线性化完全,转化背景低。建议使用。
- 单酶切线性化:线性化程度较差。可适当延长酶切时间以降低转化背景。
- 不含插入片段的假阳性克隆可能是由未线性化环状载体转化而形成的。若这种假阳性克隆比例较高,建议重新制备线性化载体。
- 双酶切线性化:线性化完全,转化背景低。建议使用。
- 反向PCR扩增制备线性化载体
建议使用高保真聚合酶进行载体扩增,以减少扩增突变的引入。PCR扩增模板应尽量使用预线性化质粒,以防止残留环状质粒模板对克隆阳性率的影响。
HiperClone重组反应体系兼容几乎所有酶切反应体系和常规PCR反应体系,当载体酶切产物或反向PCR扩增产物纯度较高时,可以无需纯化,直接进行重组反应。但纯度较低且有可能含有未线性化环状质粒时,建议使用高质量的试剂盒对线性化载体进行胶回收纯化,以提高产物纯度并去除一部分未线性化的环状载体,有利于提高重组效率。
三、PCR扩增制备插入片段
- 设计扩增引物
HiperClone引物设计方式:通过在插入片段正、反向PCR引物的5’端引入15~25bp(不包括酶切位点)的线性化载体末端同源序列,使得插入片段PCR产物5’和3’末端分别带有与线性化载体两末端对应的完全一致的序列。
推荐使用我司无缝克隆引物设计软件(https://www.bjbalb.com/Hiper-clone/),自动生成插入片段的扩增引物。若手动设计,可参照以下实例。以在pUC18载体的EcoR I和Hind III酶切位点间插入三段基因的引物设计为例,引物具体设计方案如下:
- 首先:设计第一片段的正向扩增引物和第三片段的反向扩增引物(与载体相邻的两个插入片段)。
第一片段正向扩增引物设计方式:
5'—上游载体末端同源序列+酶切位点(可保留或删除)+第一片段基因特异性正向扩增序列—3'第三片段反向扩增引物设计方式:
3'—第三片段基因特异性反向扩增序列+酶切位点(可保留或删除)+下游载体末端同源序列—5'- 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 上游/下游载体末端同源序列为线性化载体最末端序列(用于同源重组),GC含量40%~60%为佳。
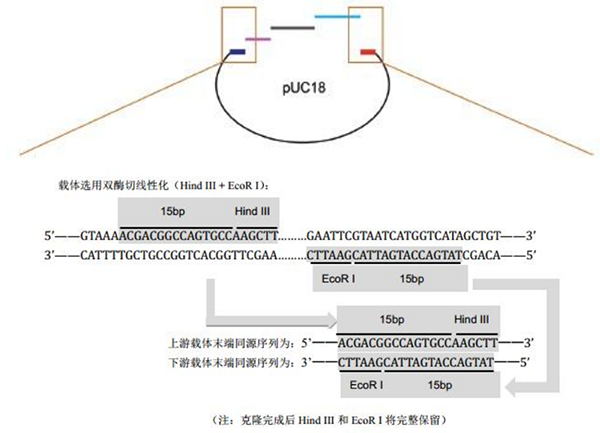
图4.与载体相邻的两个插入片段引物设计方案 - 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 其次:设计第一片段的反向扩增引物和第二片段的正向扩增引物。用于片段之间进行重组的同源序列可以添加至前方片段
的反向扩增引物中,也可以添加至后方片段的正向扩增引物中,还可以两片段各添加一部分。以将同源序列添加至前方片段
(第一片段)的反向扩增引物中为例,引物具体设计方案如图5所示:
第一片段反向扩增引物设计方式:
3'—第一片段基因特异性反向扩增序列+第二片段5'端同源序列—5'第二片段正向扩增引物设计方式:
5'—第二片段基因特异性正向扩增序列—3'- 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 第二片段5'端同源序列即用于第一片段与第二片段进行重组的添加序列。
- 基因特异性正/反向扩增序列即常规插入片段正/反向扩增引物序列;
- 最后:设计第二片段的反向扩增引物和第三片段的正向扩增引物。设计方式与第一片段的反向扩增引物和第二片段的正向扩增引物设计方式一致。具体方案参见图5。
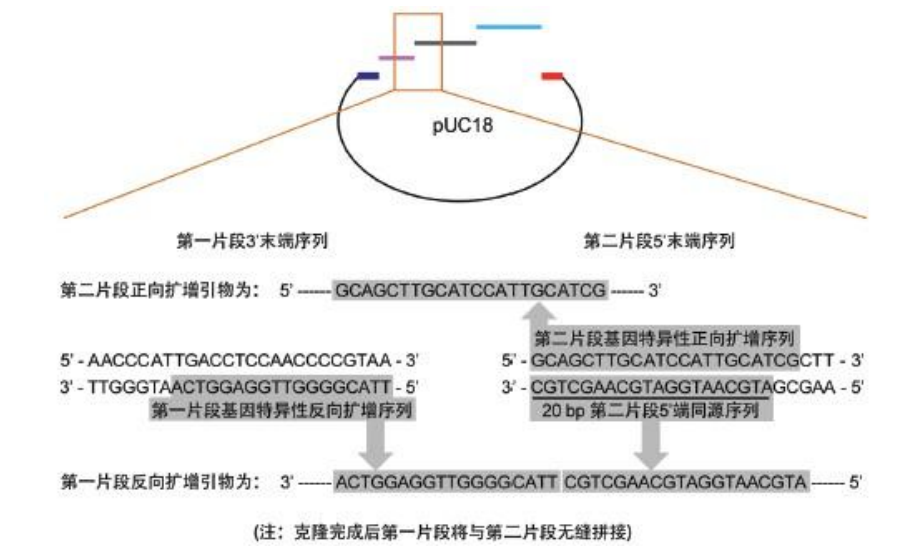
图5.第一片段的反向扩增引物和第二片段的正向扩增引物设计方案- 最终引物长度超过40bp,建议选用PAGE纯化方式进行引物合成。计算扩增引物退火温度时,只需计算基因特异性扩增序列的Tm值,载体末端同源序列不应参与计算,为了得到高效率克隆,建议Tm≥48℃。
- 首先:设计第一片段的正向扩增引物和第三片段的反向扩增引物(与载体相邻的两个插入片段)。
- 插入片段PCR扩增
插入片段扩增可用任意PCR酶扩增,无需考虑产物末端有无A尾(重组过程中将被去除,在最终载体中不会出现)。但为了减少扩增突变的引入,建议使用高保真聚合酶进行扩增。
PCR扩增结束后,取少量产物进行琼脂糖凝胶电泳以检验扩增产量和特异性。HiperClone重组反应体系兼容常规PCR反应体系。因此,如果扩增模板不是与载体抗性相同的环状质粒,且PCR产物电泳条带单一,则扩增产物可以无需纯化,直接用于重组反应。但PCR扩增产物纯度较低时,建议使用高质量的试剂盒对PCR扩增产物进行胶回收纯化,以提高产物纯度,有利于提高重组效率。

推荐使用琼脂糖凝胶电泳比较条带亮度的方法对DNA进行定量。将线性化载体和插入片段扩增产物做数个等体积稀释梯度,原始产物和稀释后产物各取1μL进行琼脂糖凝胶电泳,与DNA Marker比较条带亮度以确定其近似浓度(尤其针对于线性化载体和插入片段扩增产物未纯化的情况)。也可通过核酸浓度测定仪对线性化载体和插入片段进行测定,记录浓度值(ng/μL)和OD260/OD280值后进行投入量的计算。

- 线性化载体与插入片段使用量
HiperClone重组反应体系最适片段及载体插入总量为0.02~1pmol,1~3片段为0.02~0.5pmol,4~6片段为0.5~1pmol。最适载体与插入片段摩尔比为1:3。对应的DNA质量可由以下公式计算获得:线性化载体使用量ng =(线性化载体碱基对数×0.65×总pmol)/(1+3n)插入片段使用量ng =(插入片段碱基对数×0.65×总pmol×3)/(1+3n)
其中n表示插入片段数目。- 当插入片段长度大于载体时,最适载体与插入片段使用量的计算方式应互换,即插入片段当做载体,载体当做插入片段进行计算。线性化载体及插入片段的使用量最低可达到5ng。线性化载体和插入片段扩增产物未纯化,直接使用时,使用总体积应不超过反应体系体积的1/5,如20μL体系不超过4μL。
案例:以插入4片段(P1,P2,P3,P4),载体及片段总量为0.5pmol为例:分别将长度为0.5kb,1kb,2kb和3kb的插入片段克隆至长度为5kb的载体时,线性化载体的最适使用量应为:(5000×0.65×0.5)/13 = 125ng;插入片段P1最适使用量应为:(500×0.65×0.5×3)/13 = 37.5ng;插入片段P2最适使用量应为:(1000×0.65×0.5×3)/13 = 75ng;插入片段P3最适使用量应为:(2000×0.65×0.5×3)/13 = 150ng;插入片段P4最适使用量应为:(3000×0.65×0.5×3)/13 = 225ng。 - 重组反应体系(推荐冰上配制,各组分使用前需混匀)
成分 重组反应1~3片段 重组反应4~6片段 阴性对照 ddH2O 至20μL 至20μL 至20μL 2×HiperClone Universal Enzyme Premix 10μL 10μL 0μL 片段总量 0.02~0.5pmol 0.5~1pmol X μL - 重组反应条件
- 体系配制完成后,用移液器轻轻吸打混匀各组分,短暂离心将反应液收集至管底。
- 当插入1个片段并且DNA总量<300ng时,反应条件为50℃,5min;当插入片段数为2~6个时,建议反应条件为50℃,15~60min(反应时间随片段数增多而延长)。建议在PCR仪或金属浴等温控精确的仪器上进行反应。
- 反应产物可直接进行转化,也可储存于-20℃,待需要时解冻转化。
- 体系配制完成后,用移液器轻轻吸打混匀各组分,短暂离心将反应液收集至管底。

- 在冰上解冻克隆感受态细胞。
- 取10μL冷却重组产物,加入到100μL感受态细胞中,轻弹管壁数下混匀,在冰上放置25min。
- 42℃热激50sec,冰浴孵育1~2min。
- 加入750μL SOC或LB培养基,37℃孵育2min充分复苏。37℃,200rpm,摇菌60min。
- 5000rpm离心3min,弃掉750μL上清。用剩余培养基将菌体重悬,用无菌涂布棒在含有正确抗性的平板上轻轻涂匀。待菌液被吸收,将平板倒置,于37℃过夜培养。

最方便快捷的方法是菌落PCR。用无菌的枪头或牙签将单个菌落挑至20~50μL LB培养基中混匀,直接取1μL作为PCR模板。推荐至少用一条通用测序引物进行菌落PCR,这样可以避免PCR假阳性的产生。后续也可做酶切或测序鉴定。

- 最佳克隆位点选择?
在选择克隆位点时,应避免选择克隆位点上下游50bp内有重复序列的区域。当克隆位点上下游25bp区域内GC含量均在40%~60%范围内时,重组效率将达到最大。若高于70%或者低于30%,重组效率会受到较大影响。 - 无克隆长出或克隆数较少?
出现该情况,建议使用阳性对照,可排除试剂盒本身的影响,并进行进一步判定,主要有以下可能情况:- 引物设计不合适:推荐【同源序列(15~25bp)+完整的酶切位点+基因特异性扩增引物】,GC含量40%~60%。
- 感受态细胞效率低:使用新鲜制备或妥善冻存的感受态细胞,确保其转化效率>107cfu/μg。每次操作时可设置一组转化质粒的对照实验,以检测感受态细胞的转化效率。连接产物体积不应超过感受态细胞体积的1/10,否则会降低转化效率。
- 线性化载体和插入片段扩增产物的使用量不足/过量,或者比例不佳:尽量按照推荐的量和比例配制重组反应体系。
- 线性化载体和插入片段扩增产物不纯,抑制反应:线性化载体和插入片段扩增产物未纯化,直接使用时,使用总体积应不超过反应体系体积的1/5,如20μL体系不超过4μL。建议线性化载体、插入片段扩增产物进行凝胶回收纯化,纯化产物溶解在ddH2O中。
- 引物设计不合适:推荐【同源序列(15~25bp)+完整的酶切位点+基因特异性扩增引物】,GC含量40%~60%。
- 出现较多假阳性
- 载体线性化不完全:即使是痕量未完全酶切的载体也会产生很高的转化背景。可通过阴性对照检测载体是否线性化完全,优化酶切体系,提高限制性内切酶使用量、延长酶切反应时间、胶回收纯化酶切产物等都可以有效减少环状质粒残留。
- 插入片段扩增产物混有非特异扩增产物:建议:
- 优化PCR体系,提高特异性;
- 胶回收PCR产物;
- 鉴定更多克隆。
- 优化PCR体系,提高特异性;
- 反应体系中混入了相同抗性的质粒:PCR扩增模板(载体或插入片段)为环状质粒时,若扩增产物直接用于重组反应,残留环状质粒模板会产生较高的转化背景。建议使用预线性化质粒作为扩增模板、扩增产物进行DpnI消化或扩增产物进行胶回收纯化。
- 载体线性化不完全:即使是痕量未完全酶切的载体也会产生很高的转化背景。可通过阴性对照检测载体是否线性化完全,优化酶切体系,提高限制性内切酶使用量、延长酶切反应时间、胶回收纯化酶切产物等都可以有效减少环状质粒残留。
- 菌落PCR无条带
- 引物不正确:推荐使用载体的通用引物或至少使用一条通用引物进行菌落PCR检测。
- PCR体系或程序不合适:没有目的条带也没有空质粒条带,建议优化PCR体系、程序;或者提取质粒,以质粒做模板PCR验证;或者进行酶切验证。
- 重组失败:没有目的条带,只有空质粒的条带,说明重组不成功,载体线性化不完全,建议优化酶切体系。
- 引物不正确:推荐使用载体的通用引物或至少使用一条通用引物进行菌落PCR检测。
相关搜索:一步法同源重组克隆试剂盒,HiperClone Universal One-Step Cloning Kit



